Los procesos electroquímicos son reacciones redox en las cuales la energía liberada por una reacción espontánea se convierte en electricidad o la energía eléctrica se aprovecha para provocar una reacción química no espontánea.
Las reacciones redox son aquellas en las que se transfieren electrones de una sustancia a otra.
Una celda electroquímica es un dispositivo experimental para generar electricidad mediante una reacción redox (celda galvánica o voltáica).
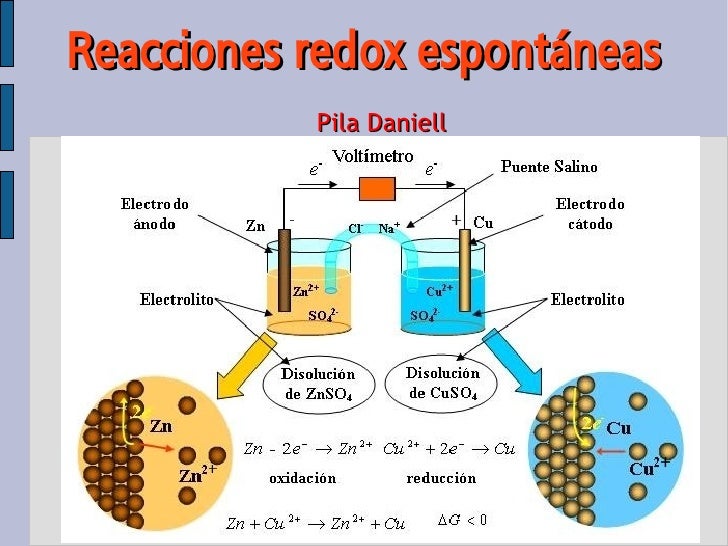
En la figura se muestran los componentes de una celda galvánica que corresponde a la celda de Daniell Zn | Zn+2 (1 M) || Cu+2 (1 M) | Cu Ánodo (+) Cátodo (-) Oxidación Reducción Pierde e - Gana e - Reductor Oxidante Reacciones de las semiceldas: Zn Zn+2 + 2 e - Cu+2 + 2e - Cu.
En una celda, el ánodo es por definición, el electrodo donde se lleva a cabo la oxidación, y el cátodo es el electrodo donde se lleva a cabo la reducción.

No hay comentarios:
Publicar un comentario